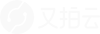王松林, 李永祥, 任 君
(中北大学化学工程与技术学院,山西 太原 030051)
对硝基苯甲酸是一种重要的有机中间体,简称PNBA(p-nithbenzoic acid),淡黄色晶体或粉末,熔点239 ℃~242 ℃,在医药领域有着广泛应用,例如,用于生产盐酸普鲁卡因、普鲁卡因胺盐酸盐,对氨甲基苯甲酸、叶酸、苯佐卡因、退嗽、头孢菌素V、贝尼尔等[1]各种医药品。它也可以用于生产活性艳红M-8B、活性红紫X-2R、滤光剂、彩色胶片成色剂、金属表面除锈剂、防晒剂等化工产品。当今,工业上对硝基苯甲酸(PNBA)主要是由对硝基甲苯(PNT)氧化生产的,氧化剂包括高锰酸钾、重铬酸钾、次氯酸钠和硝酸等。
于澍等[2]以KMnO4为氧化剂,用相转移催化氧化法合成对硝基苯甲酸,其中,十六烷基三丁基溴化磷的催化效果最好,得率达76.6%。邵啸等[3]在酸性介质中90 ℃下以KMnO4、PEG-200为氧化催化体系,KMnO4与对硝基甲苯摩尔比为3∶1,对硝基苯甲酸得率达47.25%。高锰酸钾氧化法条件温和、时间短,但是成本高、“三废”多,违背绿色化学理念,现仅用于实验室制备对硝基苯甲酸。
袁知舜等[4]小试了硝酸氧化工艺,他们控制反应条件为对硝基甲苯与硝酸的摩尔比1∶2.2~1∶4.0,20%~45%硝酸,反应温度150 ℃~220 ℃,反应压力1 MPa~4 MPa,反应时间0.5 h~2 h,对硝基苯甲酸得率可达95%。硝酸氧化法虽然工艺简便、成本低廉,但是由于生产中使用稀硝酸对设备腐蚀严重,反应产生的NOx是形成酸雨的主要气体,故此种方法也受到严格限制。
空气氧化法是近年发展的生产工艺,该氧化法就是利用空气或氧气在液相中氧化[5-6]PNT生产PNBA,主要分为酸法和碱法,以使用介质的酸碱性进行区分。马玉龙等[7]以芳烃为溶剂,加入自制催化剂,直接用空气氧化PNT,PNBA得率可达94.55%。高敏等[8]以邻二氯苯-丙酸作溶剂,在乙酸钴、溴化物复合催化剂催化下,用空气氧化PNT合成PNBA,并对反应条件进行研究,PNBA得率可达90.4%。
综上所述,目前工业生产制备对硝基苯甲酸的工艺均有环境污染和设备腐蚀的缺陷[9-10]。因此,探究一种条件温和、环境友好的对硝基苯甲酸制备工艺十分有必要,具有一定现实意义。本文采用的氧化剂氯酸钠中不含重金属离子,反应液对设备腐蚀轻微,有助于减少维护成本,废液后处理成本低廉,是一种良好的对硝基苯甲酸制备工艺。
1 实验材料、试剂及仪器1.1 材料及试剂对硝基甲苯,甘肃银光化学工业集团有限公司。
98%浓硝酸,天津市化学试剂研究所;氯酸钠,国药集团化学试剂有限公司;98%浓硫酸,天津市化学试剂研究所;苯,天津市申泰化学试剂有限公司;丙酮,天津申泰化工试剂;冰醋酸,西陇科学股份有限公司;无水甲醇,天津市天力化学试剂有限公司;氢氧化钠,天津市大茂化学试剂厂。
1.2 仪器SHZ-CA循环水式多用真空泵,巩义市予华仪器有限公司;FTIR-7600红外光谱仪,天津分析仪器厂;WRX-4熔点仪,上海易测仪器设备有限公司。
2 实验方法本实验以对硝基甲苯为原料,氯酸钠作为氧化剂,合成路线如式(1)所示。
在装有冷凝器、温度计、搅拌器的四口烧瓶中,称量5 g对硝基甲苯、加入10 mL98%浓硝酸,开启水浴、搅拌(500 r/min左右),直至其升温至80 ℃。称量9.72 g氯酸钠溶于10 mL蒸馏水制成饱和溶液,移入恒压滴液漏斗,撤掉冷凝器,缓慢滴加2滴~3滴氯酸钠饱和溶液,待烧瓶内黄绿色变淡时,再滴加2滴~3滴氯酸钠的饱和溶液,如此反复,直至滴加完毕。待反应温度降至80 ℃左右开始计时,水浴(或油浴)保温。4 h后停止反应,继续搅拌,待烧瓶内温度降至常温后,将反应液倒入100 mL冰水混合物中,冰块融化后抽滤,抽滤所得滤渣再次水洗抽滤,如此反复3次,所得滤渣即为对硝基苯甲酸粗品。
2.2 对硝基苯甲酸粗品的提纯将上一步所得的对硝基苯甲酸加入烧杯中,加入30 mL蒸馏水,进行磁力搅拌,缓慢滴加15%NaOH溶液,直至液体呈现红色,停止滴加NaOH溶液,静置30 s,溶液不褪色即开始下一步,若中途褪色则继续滴加NaOH溶液。所得溶液继续搅拌,缓慢滴加无水乙酸,直至溶液褪色且30 s内不变回原来的颜色,所得液体抽滤,滤渣即为此次提纯的杂质,杂质应该包括未反应的对硝基甲苯及其他副产物。滤液进行磁力搅拌,缓慢滴加50%稀硫酸,直至无明显沉淀生成,所得液体抽滤,滤渣即为较纯的对硝基苯甲酸,所得滤液回收,重复滴加50%稀硫酸,如有产品则抽滤,如此重复3次。将滤出产物于50 ℃烘箱中进行干燥,称量,计算得率。
3 结果与分析3.1 产物的表征产品外观为淡黄色晶体,通过熔点测定,得出其初熔点为234.1 ℃,终熔点为235.9 ℃,与文献报道基本相符。
3.1.1 薄层色谱分析
对所得产物进行薄层色谱分析(TLC),TLC条件为乙醇为溶剂,n(苯)∶n(丙酮)∶n(冰醋酸)∶n(甲醇)=5∶1∶1∶1为展开剂,硅胶板上只有一个聚集不发散的点。
3.1.2 红外光谱测试
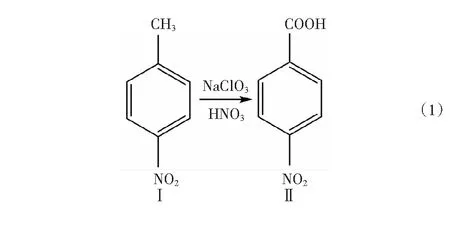
图1为对硝基苯甲酸的红外光谱图。
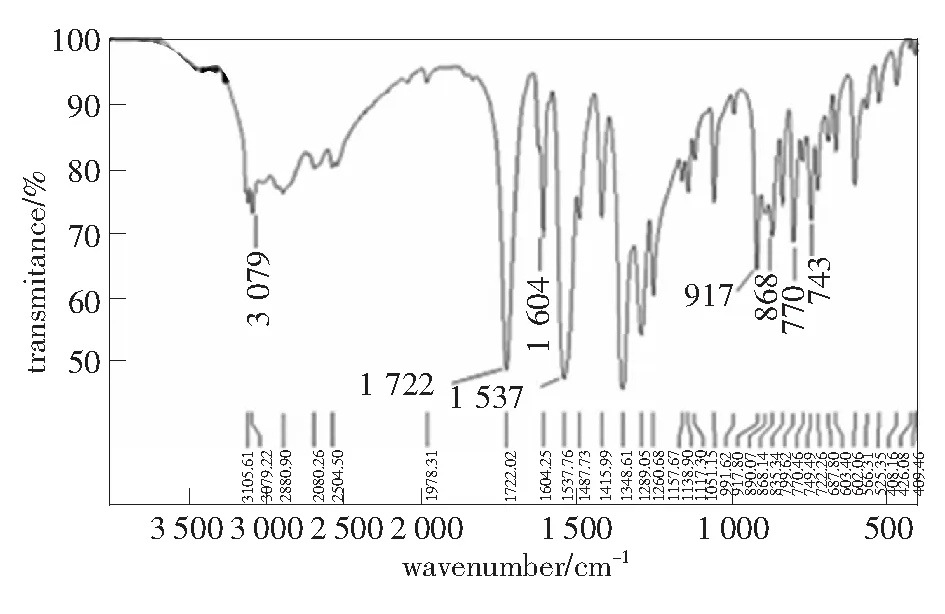
图1 对硝基苯甲酸的红外光谱图
图1中,3 105.61、3 079.22、2 880.90 cm-1有弱吸收存在,为苯环上C-H伸缩振动;1 604.25、1 537.76、1 487.73 cm-1有中强吸收峰存在,为苯环C=C的骨架振动;890.07、868.14、770.46、743.49 cm-1有吸收,为苯环上C-H面外弯曲振动;1 537.76、1 317.73、565.31 cm-1有吸收表明有C-NO2存在;3 500 cm-1~2 500 cm-1的宽吸收峰为游离羧酸的O-H伸缩振动、1 722.02 cm-1处为C=O伸缩振动、917.80 cm-1处为O-H弯曲振动,表明有-COOH存在。根据谱图分析的结果可以确定该物质为对硝基苯甲酸。
3.2 对硝基甲苯制备对硝基苯甲酸的工艺优化3.2.1 反应物摩尔比对PNBA得率的影响
以对硝基甲苯5 g,反应时间为4 h,反应温度为80 ℃左右为例,考察对硝基甲苯与氯酸钠摩尔比对PNBA得率的影响,单因素实验结果如第3页图2。
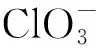
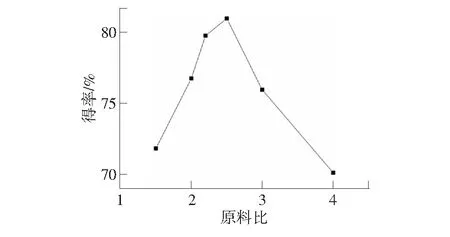
图2 反应物摩尔比对PNBA得率的影响
3.2.2 反应时间对PNBA得率的影响
以对硝基甲苯5 g,反应料比(对硝基甲苯与氯酸钠摩尔比)1∶2.5,即,9.72 g氯酸钠溶于10 mL蒸馏水制成氯酸钠的饱和溶液作为氧化剂,反应温度80 ℃左右为例,考察反应时间对PNBA得率的影响,单因素实验结果如图3。
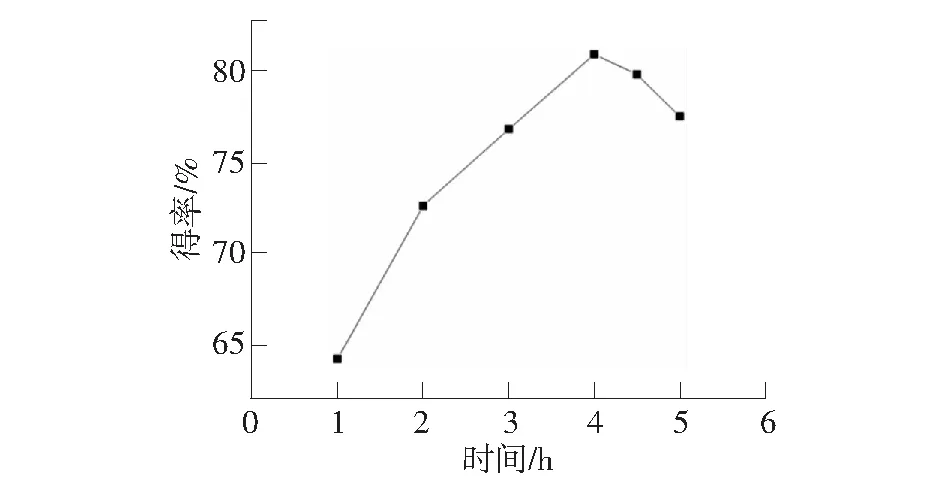
图3 反应时间对PNBA得率的影响(1)
由图3看出,随着反应时间的增加,得率先增加后降低,反应时间在4h左右,得率最大为80.9%。主要原因是,氧化过程分为多个阶段,时间太短会使反应停留在中间阶段,生成中间产物如醇、醛等。适当延长时间可以使反应物较完全地转化为羧酸,于4 h左右达到最大转化率。当反应时间过长时,由于酯化反应等副反应的存在,得率反而降低。
在4 h附近得率起伏较大,为了得到更精确的最佳反应时间,在4 h附近取新的时间点,进行几组单因素实验。以对硝基甲苯5 g,反应料比(对硝基甲苯与氯酸钠摩尔比)1∶2.5,反应温度80 ℃左右为例,在反应时间4 h附近,精确考察反应时间对PNBA得率的影响,结果如图4。
由图4看出,PNBA合成的最佳时间是4.1 h,得率为81.5%。
3.2.3 反应温度对PNBA得率的影响
以对硝基甲苯5 g,反应时间4.1 h,反应料比(对硝基甲苯与氯酸钠摩尔比)1∶2.5,考察反应温度对PNBA得率的影响,单因素实验结果如图5。
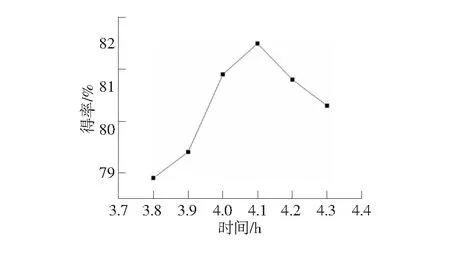
图4 反应时间对PNBA得率的影响(2)
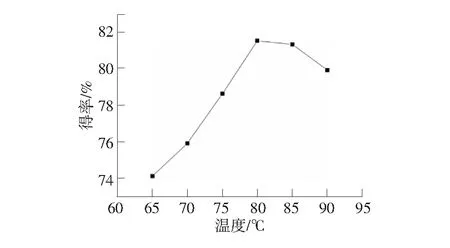
图5 反应温度对PNBA得率的影响
由图5看出,随着反应温度的增加,得率先增加后基本持平然后开始降低,反应的较佳温度范围为80 ℃~85 ℃。主要原因是,反应温度较低时不足以达到反应所需的活化能,部分分子未活化,后降低是因为反应温度过高氧化副反应加剧,气体副产物比例增加。
研究表明,合成PNBA的最佳工艺条件为对硝基甲苯与氯酸钠摩尔比1∶2.5,反应温度为80 ℃~85 ℃,反应时间4.1 h。按此实验条件进行3次,并计算其平均得率,结果如表1所示。
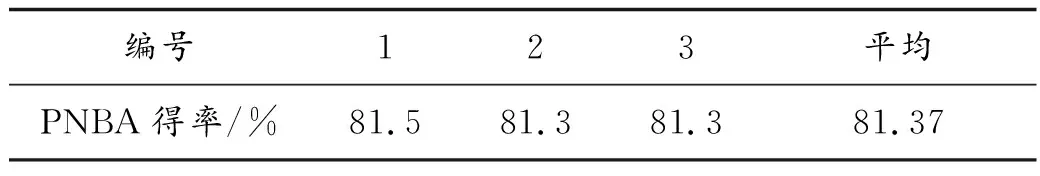
表1 单因素法最优实验条件合成PNBA得率
4 结论本文选择氯酸钠氧化对硝基甲苯制备对硝基苯甲酸,通过实验研究和产品检测,得出如下结论:
使用氯酸钠作氧化剂,通过控制原料比、时间和温度进行单因素实验,确定了制备对硝基苯甲酸的最佳工艺条件为:对硝基甲苯与氯酸钠的摩尔比1∶2.5,反应温度80 ℃~85 ℃,反应时间4.1 h,产品的得率为81.37%。并且对产物进行熔点测定、薄层色谱分析及红外光谱分析,结果表明该物质与目标产物一致。可见这是一条比较理想的对硝基苯甲酸制备途径,为放大中试进一步工业化奠定了基础。